نظرسنجی
شما
یادداشت های مهم
همهابر برچسب
انرژی های تجدید پذیر ختم قرآن/رمضان 94 ختم قرآن/قرآن/ماه رمضان/رمضان خودرو کتاب ویل دورانت لذات فلسفه ویل دورانت لذت فلسفه لذات فلسفه مجله تهویه مطبوع،تهویه مطبوع آزمون مبانی مهندسی حرفه ای روش مدیریت زمان روش های مدیریت زمان کنکور دکتری مصاحبه با رتبه برتر کنکور ارشد تمرکز برای کنکور تمرکز در مطالعه قانون پارکینسون مصاحبه با نفرات برتر کنکور ارشد مدیریت زمان مهندسی مکانیکجدیدترین یادداشتها
همه- خداحافظ
- تولدت مبارک عسل بانو
- فیلم آموزش نصب کولر اسپیلت .(زبان اصلی)
- معرفی فیلم pk
- مشکل کمبود آب برطرف شد :) واقعا !!!
- ختم قرآن عربی/فارسی رمضان 94
- یه روزی به گوشت میرسه!"
- رضایت/نعمت/ترس
- یادگیری نرم افزار کریر و شروع کار تاسیسات
- افزایش رطوبت ،کاهش دما
- محصولات چینی در زمینه انرژی خورشیدی+++
- فیلم دیگ چدنی
- یار دوازدهم کی .....
- نظر سنجی ختم قرآن /هخامنش عزیز
- مقاله cfd
- رتبه ها و درصد ها
- سنگفرش هر خیابان از طلاست
- انگشترم / هخامنش
- دانلود مجموعه آهنگهای بی کلام رویاهای عاشقانه
- توجه در نماز !
بایگانی
- تیر 1396 1
- تیر 1394 4
- خرداد 1394 10
- اردیبهشت 1394 8
- فروردین 1394 23
- اسفند 1393 8
- آذر 1393 1
- آبان 1393 4
- مهر 1393 3
- شهریور 1393 10
- مرداد 1393 29
- تیر 1393 16
- خرداد 1393 6
- اردیبهشت 1393 24
- فروردین 1393 23
- اسفند 1392 24
- بهمن 1392 9
- دی 1392 9
- آذر 1392 6
- آبان 1392 6
- مهر 1392 7
- شهریور 1392 25
- مرداد 1392 77
- تیر 1392 50
- خرداد 1392 38
- اردیبهشت 1392 3
- بهمن 1391 25
- دی 1391 5
- آذر 1391 7
- آبان 1391 10
- مهر 1391 2
- شهریور 1391 20
- مرداد 1391 23
- تیر 1391 6
- خرداد 1391 10
- اردیبهشت 1391 38
- فروردین 1391 9
- اسفند 1390 36
- بهمن 1390 5
- دی 1390 5
- آذر 1390 7
- آبان 1390 5
- مهر 1390 6
- شهریور 1390 15
- مرداد 1390 20
- تیر 1390 6
- خرداد 1390 5
- اسفند 1389 1
- بهمن 1389 2
- آذر 1389 1
- مهر 1389 1
- شهریور 1389 7
- مرداد 1389 22
- خرداد 1389 1
- فروردین 1389 8
- دی 1388 1
- آذر 1388 1
- آبان 1388 1
- مهر 1388 1
جستجو
آمار : 2861768 بازدید
Powered by Blogsky
پرسش ترمو-جایزه برای کسانی که درست جواب بدن
با ارایه یک مثال (مثال فقط مثال اونم مثال عینی توضیح کتابی نمیخوام)توضیح بدین چرا انتگرال سیکلی دلتا Q به T همواره کوچکترمساوی صفر است؟
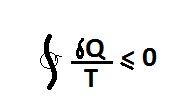
هخامنش پارسی
پنجشنبه 6 تیرماه سال 1392 ساعت 16:06
این نامساوی رو درحقیقت این آقای کلازیوس چی بگم شده که از بنیان گذارهای علم ترمودینامیک هستن اثبات کرد و با اون تونست به روابط برگشت ناپذیری ها و محاسبه اونها برسه وخلاصه خیلی کارا

این نامساوی میگه اقا همه فرایند های برگشت نا÷ذیر در جهت تولید انتروپی ÷یبش می رن حالت مساوی زمانی که فر یند ها برگشت پذیر و ایده ال هستن و لی در حالت نامساوی ما مقداری تولید انتروپی ناشی از برگشت نا÷ذیری ها رو داریم که باعث میشه این انتگرال سیکلی از مقدار مشابه آن در حالت برگشت پذیر با همان انرپی گرمایی و دمای مشخص کوچکتر باشه و نقش ds generation رو مشخص می کنه مثال هم که این همه مثال هرچی فرایند توی این دنیا فکر کنی همش مثال قانون دومه
ولی خدا ازش نگذره عجب چیزی رو کشف کرد
ممنون
دیدی بازم حرف کتابا رو تکرار کردی!
اما منظورم این بود که یکی از اینهمه مواردی که تو دنیا هست رو تشریح کنید...
مهمه...
ساده ترین مثال عینی که میشه زد موتور گرمایی،که یک وسیله سیکلی برگشت پذیر فرضش میکنم.به منبع انرژی گرمایی با دمای مطلق "ثابت" T_R متصل و گرمای Q_R را از منبع گرم میگیره و گرمای δQ را از طریق مرز سیستم که در دمای متغیر T است به سیستم میده.خب طبیعیه که کار δw رو انجام میده.موازنه انرژی را بنویسیم داریم:
δw_c=T_R (δQ/T)-δE_c
δE صفر،زیرا یک سیکل داریم و در سیکل انتگرال سیکل انرژی صفر.
سیستم رو هم برگشت پذیر فرض کردیم که در سیستم برگشت پذیر داریم:
δQ/T=(δQ_R)/T_R
پس:
W_C=T_R ∮▒δQ/T
طبق بیان کلوین پلانک هم هیچ سیستمی در یک سیکل که فقط با یک منبع انرژی گرمایی تبادل گرما داره نمیتونه مقداری کار خالص تولید کنه پس W_C نمیتونه کار خروجی باشه و کمیتی مثبت نیست.T_R هم که دمای مطلق بود و یک کمیت ثابت پس در موتور گرمایی ما :
δQ/T ≤0∮▒
این مثال برای موتور گرمایی برگشت پذیر بود.برای همه سیستم های برگشت پذیر ،برگشت پذیر داخلی و برگشت ناپذیر میشه مثال زد.یخچال،سیستم های تهویه و تبرید،کمپرسور و...
مرسی از بابت تایپ و خیلی هم ممنون
البته منظورم مثال های فیزیکی ملموس در طبیعت بود نه موتور گرمایی و استفاده از اصطلاحات مهندسی همچون بازگشت پذیر و...
در واقع یه مثال عددی میخوام مثلا یه فنجون چای داغ که در محیط خنک تر قرار میگیره این انتگرالو براش ثابت کنید...
ضمنا جایزتون به خاطر زحمت و تایپ فارسی و ریاضی قطعا سرجاشه...
خب همین فنجون قهوه داغ که خودتون گفتین رو بررسی میکنم
با اجازتون آپلودش کردم،اینجا که مینوشتم قسمت ریاضیش بهم میریخت .اگه دوست داشتین ببینید
http://s4.picofile.com/file/7835956662/%D8%AA%D9%88%D8%B6%DB%8C%D8%AD_%D9%85%D8%AB%D8%A7%D9%84_%D9%81%D9%86%D8%AC%D9%88%D9%86_%D9%82%D9%87%D9%88%D9%87.docx.html
نمیدونم جواب مدنظرتون رو دادم یا نه.
ممنون دانلود کردم و خوندم اما انتگرالی که گرفتین اصلا سیکلی نیست! سیکل یعنی سیستم(چای داغ) دوباره برگرده به حالت اولش اما شما فقط تبادل گرما با محیط و نهایتا به تعادل رسیدن با اون رو نشون دادید سعید جان.
ضمنا خط اول نیازی به عبارت یک منهای Ts نبود و نفهمیدم اصلا از کجا آوردیش...فقط کافی بود مینوشتی Ts>Tsur و ادامه...
ضمنا خط سوم هم به خاطر این صفر شده که Ts=Tsur و طبیعتا انتقال گرما صفر میشه و بازم نفهمیدم عبارت 2 منهای Ts رو از کجا اوردی!
مهندس اون خط تیره بود نه منها
1 یعنی حالت اول و 2 یعنی حالت دوم
مثل اینکه جواب مدنظر شما رو نمیتونم بدم
در هر صورت مرسی
آها خط تیره بوده...اوکی البته در خط دوم باید مینوشتید Ts/Tsur<1 نه صفر...که احتمالا اشتباه لپّی بوده !!
در هر صورت تحلیلی که داشتی بسیار بسیار ارزشمند اما به سیکل اشاره نمیکنه و صرفا فراینده در صورتیکه
چیزی که مدنظر ماست ارایه مثال برای یک سیکله...
سعید جان ارشد میخونی؟یا براش آماده میشی؟چی بدردت میخوره به عنوان جایزه نآقابل برادر؟
خواهشا تعارف هم نکن.این وظیفه منه
مهر دانشجو میشم.
قطعا هدفم یادگیری مهندس.جایزه و این حرفا مال سن 20 سال پیش من.به خاطر همین هیچ آدرسی از خودم نذاشتم.تازه جوابمم که درست نبود.
همین که موضوعی مطرح بشه دنبال جوابش برم کافیه.بازم پیگیر جواب هستم!
خیلی ام ممنون که مسائل رو مطرح میکنید.
انشالّله
درود بر شما